
세포막 단백질을 분리하기 위해 단백질을 용해할 수 있는 detergent (세정제)를 사용합니다.
세포를 lysis(용해)시킬 때 사용하죠.
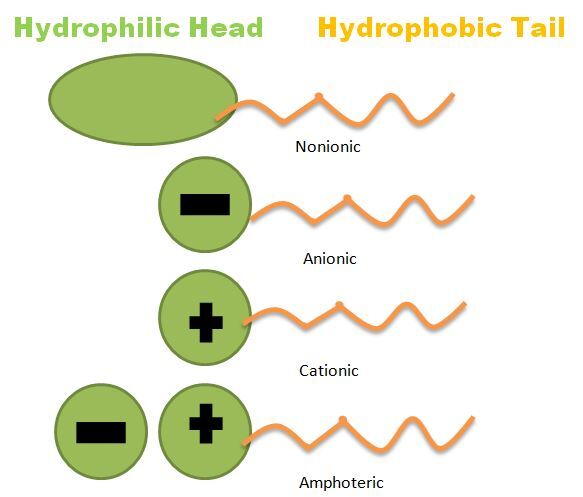
각 detergent는 hydrophilic head에 따라 다음과 같이 나눌 수 있습니다.
| Detergent | Effect |
| Ionic (이온성) |
Membrane을 쉽게 분산시키지만 모든 protein을 파괴하는 성질 (예: Sodium dodecyl sulfate(SDS), Lithium dodecyl sulfate(LDS)) |
| Non-Ionic (비이온성) |
- 0.1% 이하의 일정 농도에서 protein 변성을 초재하지 않으므로 기능을 유지한 단백질 분리에 사용하지만 단백질 응고가 일어날 수 있음. 영향을 미치지 않으며, lipid membrane만을 파괴함. (예: Triton X-100, NP-40, Tween-20) |
| Amphionic (양수성) |
가용화 능력이 강하고, 단백질 변성이 적음. pH 7.0 이하가 되면 용해도가 낮아짐. (예: CHAPS, Zwitterionic 세정제) |
*ELISA 측정 시 사용하는 일반적인 PBST용액
→ (1x PBS에 0.05 %(v/v) Tween-20)
CMC (임계 미셀 농도)
Detergent을 잘 활용하기 위해서는 CMC를 알아야 합니다.
CMC를 경계로 하여 이 이전 농도에서는 detergent는 역할을 하지 못하며, 이 농도를 넘어서야 제 역할을 하기 때문입니다.
Critical micelle concentration(CMC)은 각 세정제가 micelle을 형성하는 최저 농도입니다.
Hydrophobic tail 때문에 물속에 존재하기 힘든 detergent들이 물 표면부터 배열하기 시작하고, 물 표면을 다 채운 후에는 더 이상 표면에 존재하기 힘들기 때문에 micelle을 형성하게 됩니다.
이때, 처음 micelle (미셀)을 형성할 때의 농도를 CMC라고 하는 것이죠.

계면활성제가 용액 내에서 micelle을 형성하면 무슨 일이 생길까?
Detergent가 micelle을 형성하면 정상적으로 용해되지 않는 제3의 물질을 micelle 내부에 용해시킬 수 있는 성질을 가지게 됩니다.
이러한 현상을 solublization이라 합니다.
일반적으로, 비이온성 계면활성제는 동일한 탄화수소 chain일 경우 이온성계보다 낮은 CMC를 가지므로 용해능이 크며, 그 순서는 비이온성 > 양이온성 > 음이온성의 순서이다.
예를 들어, 매우 낮은 CMC를 가진 Tween-20은 일반적으로 면역화학법 (ELISA 등)에서 단백질의 비특이적 반응을 억제하기 위해 사용합니다.
반면,
Zwitterionic 세정제는 상대적으로 높은 CMC를 가지고 있기 때문에 비이온성 세정제보다 단백질-단백질 상호작용을 극복하면서 이온성 세정제보다는 단백질의 변성을 덜 초래합니다.
+) 추가
* CMC 농도
| Detergent | CMC | 종류 및 특징 |
| SDS | 8.2 mM at 25 ℃ | 음이온성 계면활성제 |
| Triton X-100 | 0.22 mM | 비이온성 계면활성제 |
[Reference]
- 위키백과
https://www.ipcol.com/blog/an-easy-guide-to-understanding-surfactants/
- 계면활성제의 기본 물리화학적 성질
: https://www.cheric.org/files/research/symposium/S-C1-0079.pdf
'Experiment > Biochemistry Experiment' 카테고리의 다른 글
| [ELISA] Biotin을 이용한 signal 증폭 (Biotin Signal Amplification) (0) | 2023.07.31 |
|---|---|
| [단백질] 단백질 연구 시 고려해야 할 사항 4편_단백질 환경 (Protein enviroment) (0) | 2023.06.13 |
| [단백질] 단백질 연구 시 고려해야 할 사항 2편_환원제 (Reducing agents) (0) | 2023.05.25 |
| [단백질] 단백질 연구 시 고려해야 할 사항 1편_완충용액 (Buffers) (0) | 2023.05.23 |
| [발현] Inclusion body (Insoluble form protein) (0) | 2023.05.17 |



